高效伤口敷料的开发对于成功的临床应用至关重要,特别是对于需要快速愈合和最小化疤痕的感染伤口。近日,山东医药大学(原滨州医学院)侯桂革/李诚博在《Chemical Engineering Journal》(IF=13.2)发表研究论文“Skin temperature-activated shape memory bilayer scaffolds for scarless infected wound healing”,在这项研究中,成功开发了一种具有温度激活形状记忆特性的新型双层伤口敷料(CFCQS)。外层纤维层由聚(L-丙交酯-共聚三亚甲基碳酸酯)(PLATMC)组成,具有温度触发卷曲和疏水抗菌特性,而内层胶原蛋白(COL)/季铵化硅酮(QP12)海绵层则具有抗菌和抗炎功能,促进无疤痕伤口愈合。体内实验表明,CFCQS能有效促进血管生成、调节炎症因子表达并加速伤口闭合,为增强伤口愈合效果提供了一种有前途的解决方案。
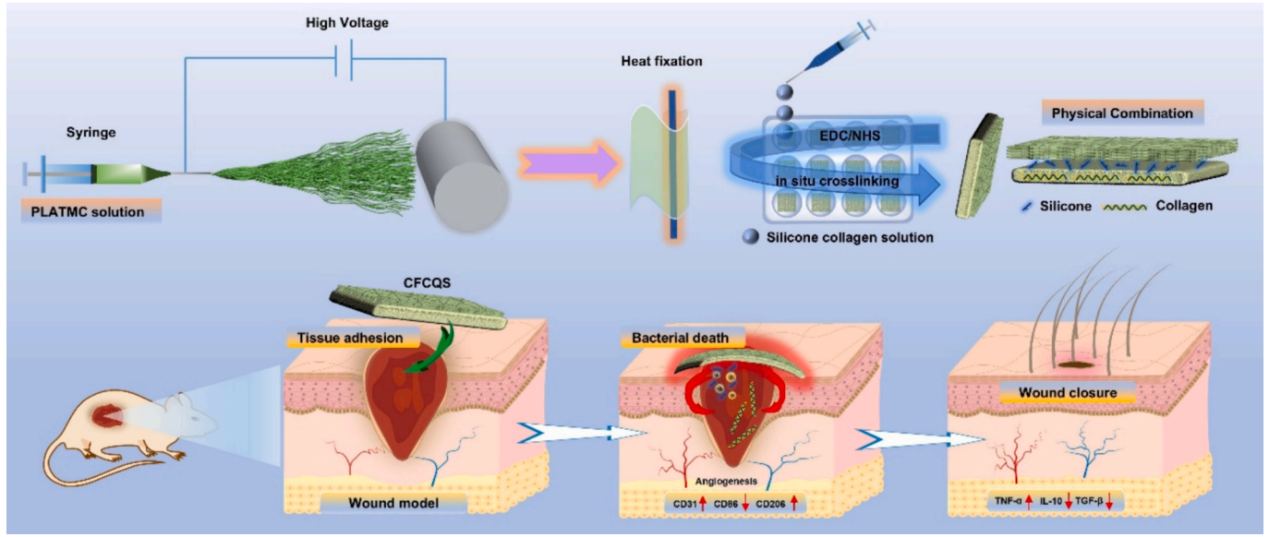
示意图:具有温度响应性机械收缩特性、抗菌和抗炎特性的CFCQS的制备及作用机制示意图。采用静电纺丝技术制备PLATMC纤维,通过热固定方法进行形状记忆。海绵层溶液在其上方通过EDC/NHS进行原位交联后冻干,最终获得该双层敷料,通过开发CFCQS来协同PLATMC纤维的温度激活形状记忆效应与胶原/季铵化硅酮海绵的抗菌和免疫调节特性。该设计不仅通过热收缩促进伤口快速闭合,还能积极解决感染、抑制纤维化。
一、结构与温敏特性拉满,理化性能全面适配
图1与图2共同展现了敷料的微观结构、温敏形状记忆性能与核心理化指标。外层PLATMC静电纺纤维膜形貌均匀,内层胶原/季铵化硅酮海绵多孔互联,季铵化硅元素均匀分散,在37℃体温下可触发自主卷曲收缩,为伤口提供机械闭合助力;红外光谱证实材料成功交联,孔隙率65%–69%、溶胀率约470%,耐热性优异,吸液、结构稳定性完全贴合伤口敷料使用需求。
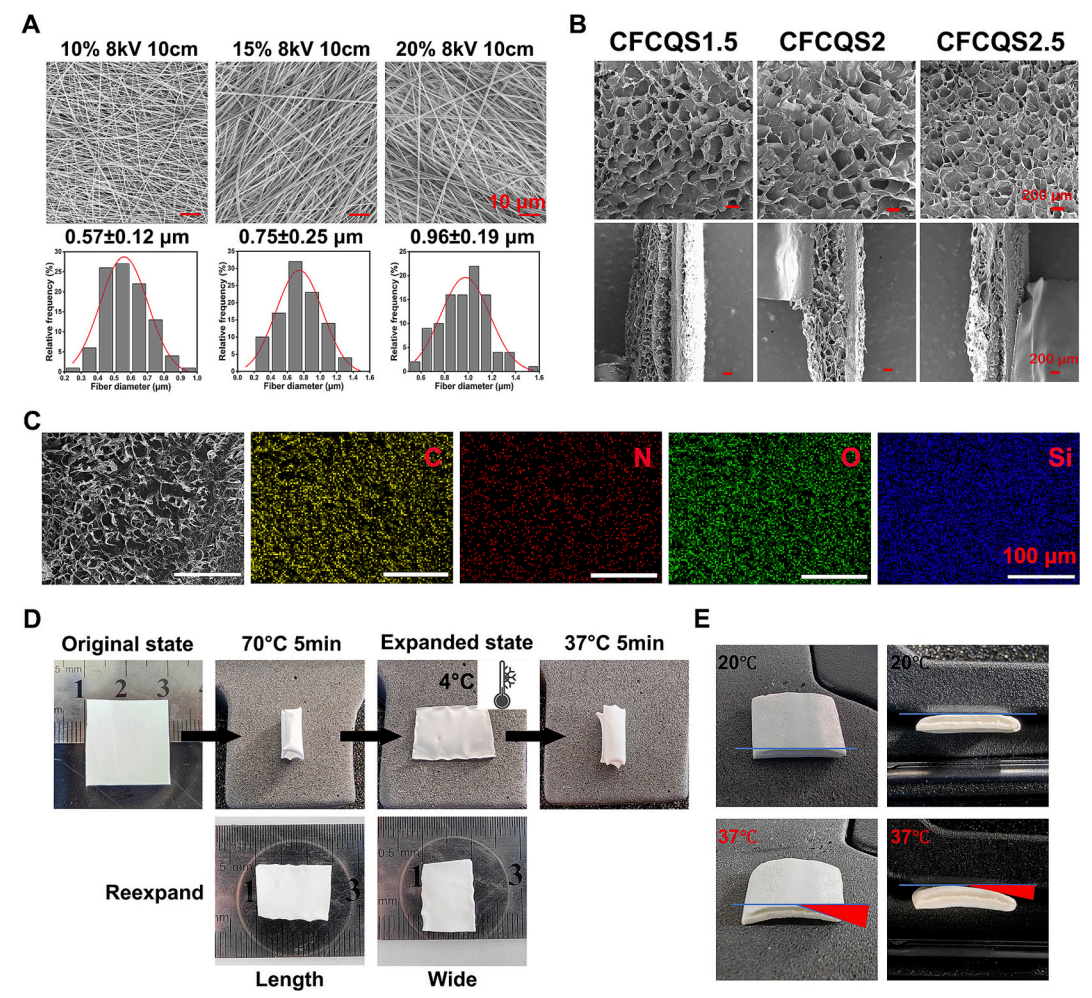
图1. 电纺PLATMC纤维膜和胶原基季铵化硅酮复合海绵的形态表征。(A) 在固定静电纺丝参数(8 kV电压,10 cm距离)下以不同聚合物浓度(10%、15%和20%,w/v)制备的电纺PLATMC纤维膜的SEM图像和纤维直径分布直方图。(B) 季铵化硅酮浓度不断增加的复合海绵(CFCQS1.5、CFCQS2和CFCQS2.5)的表面形貌(上排)和横截面结构(下排)。(C) CFCQS海绵中碳、氮、氧和硅的SEM图像和相应的EDS元素图,表明季铵化硅酮的均匀分布。(D) 热形状记忆固定后纤维膜在37°C下的温度响应测试。(E) 纤维膜-海绵复合材料在37℃下的热弯曲图像。
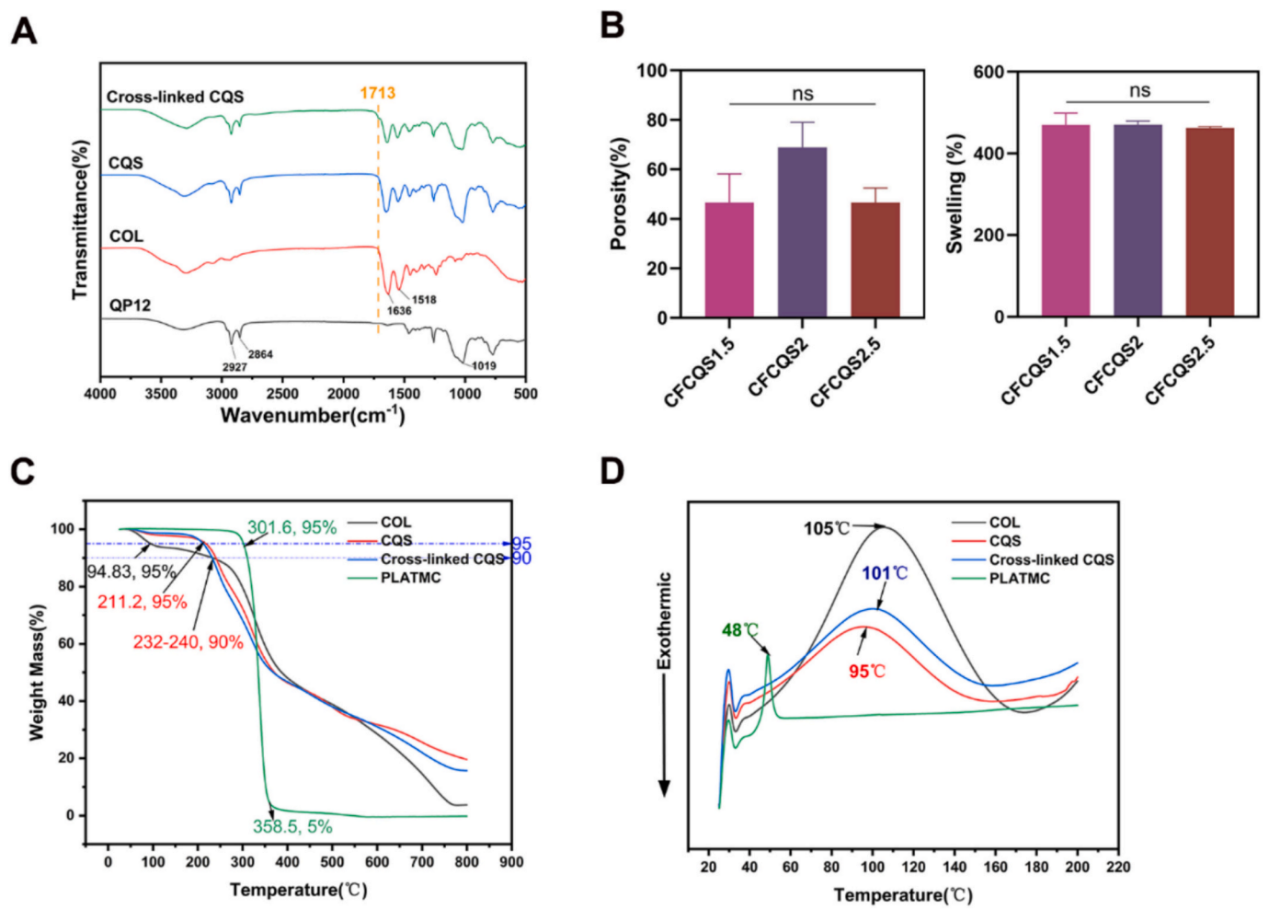
图2. 胶原基季铵化硅酮复合海绵的物理化学表征。(A) 傅里叶变换红外光谱证实复合海绵内的化学相互作用和交联。(B) CFCQS复合海绵(CFCQS1.5、CFCQS2和CFCQS2.5)的孔隙率和膨胀率(%)。“ns”表示没有显著差异。(C) 热重分析(TGA)曲线,描绘胶原(COL)、非交联胶原季铵化硅酮(CQS)、交联胶原季化硅酮(Cross-linked CQS)和PLATMC纤维膜的热稳定性和分解行为。(D) 差示扫描量热法热分析图显示与胶原变性和复合材料组件热转变相关的特征吸热峰。
二、生物安全抗菌止血,创面愈合速度领跑
图3与图4聚焦敷料的生物安全性、抗菌止血能力与在体愈合效果。细胞实验证实敷料无毒性、生物相容性达标,对金黄色葡萄球菌、大肠杆菌均有显著抑菌作用,体外与在体止血表现突出;小鼠全层感染创面实验中,CFCQS2组伤口闭合更快、感染控制更佳,14天愈合率达98.1%,伤口边缘体温持续激活温敏收缩,全程无明显疤痕。
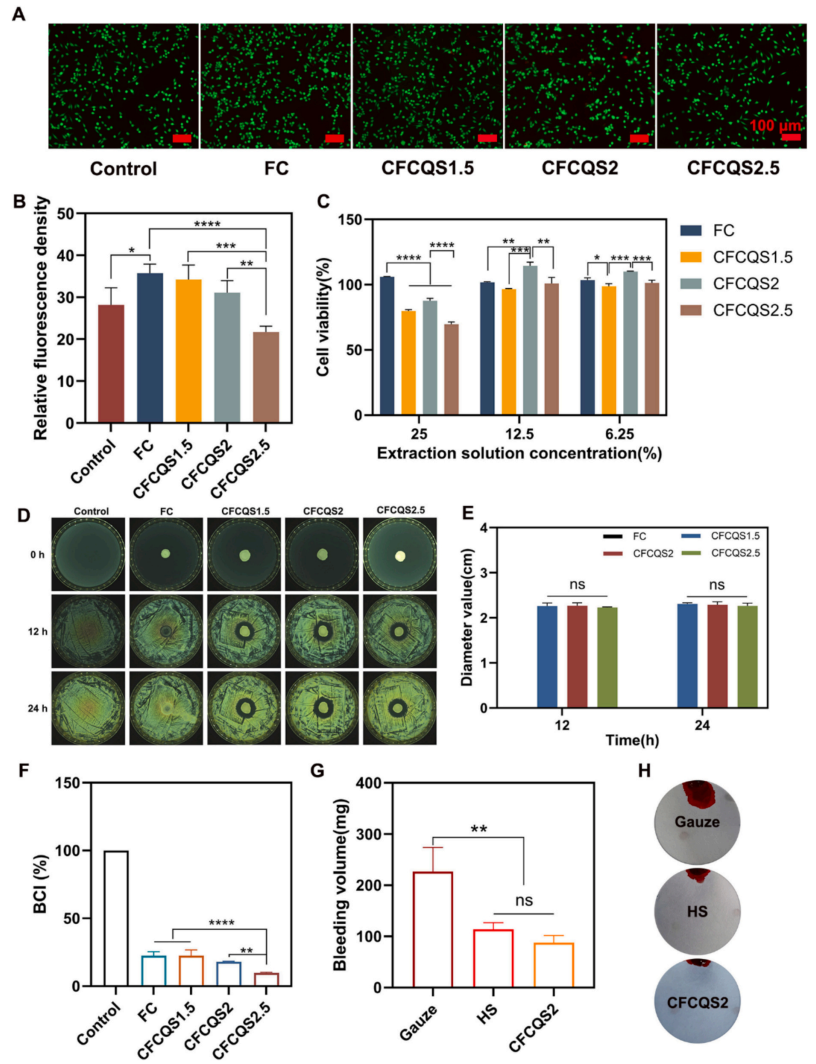
图3. CFCQS复合敷料的细胞相容性、抗菌活性和止血评价。(A) 活/死染色的荧光图像。(B) 相对荧光密度的定量表明用复合海绵培养的L929细胞的活力有所提高。(C) 暴露于不同提取溶液浓度(25%、12.5%和6.25%)的L929细胞的细胞活力测定。(D) 通过0、12和24小时的金黄色葡萄球菌抑制区评估敷料的抗菌活性。(E) 抑制区直径的量化(ns表示没有显著差异)。(F) 凝血指数分析证实有效的凝血特性。(G) 小鼠肝出血模型中的体内出血量测量。(H) 显示纱布、市售止血海绵(HS)和CFCQS2敷料吸收血液的代表性图像。统计显著性:*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001。
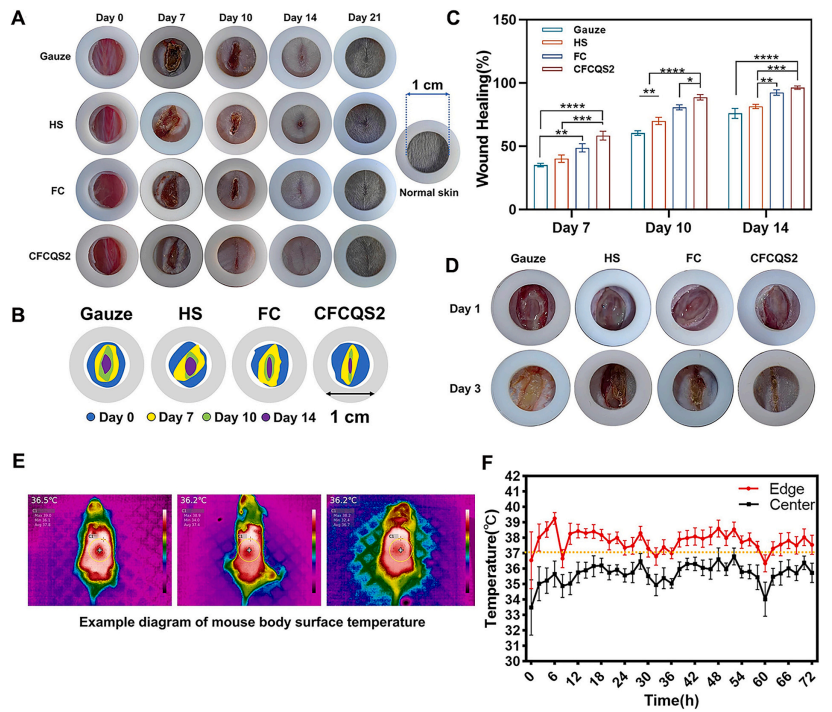
图4. CFCQS复合敷料的体内伤口愈合功效和温度响应性。(A) 使用纱布、商用止血海绵(HS)、纤维复合材料(FC)和CFCQS2敷料治疗21天内伤口愈合进展的代表性宏观图像。提供正常皮肤图像作为参考。(B) 轮廓示意图显示了每个治疗组从第0天到第14天的伤口闭合进展。(C) 治疗后第7、10和14天伤口愈合百分比的定量分析。(D) 代表性图像显示每种敷料在感染后第1天和第3天的感染控制功效。(E) 红外热成像图像显示不同时间点伤口部位的小鼠背表面温度。(F) 72小时内伤口边缘和中心温度变化的时程监测(n = 11)。边缘温度保持在37°C以上,支持温度触发的敷料变形。统计显著性:*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001。
三、组织修复+免疫调控,从根源实现无痕愈合
图5至图8完整揭示敷料深层修复与抗疤痕核心机制。组织染色显示,CFCQS2组再上皮化更快、胶原排列规整,皮肤厚度与胶原比例最终回归正常水平;免疫荧光与组化证实,敷料可显著促进血管生成,驱动巨噬细胞从促炎M1型向修复M2型转化,下调TNF-α、上调IL-10,并持续抑制疤痕关键因子TGF-β过度表达,从炎症调控、胶原重塑到抗纤维化全链路优化,真正实现感染创面的无痕修复。
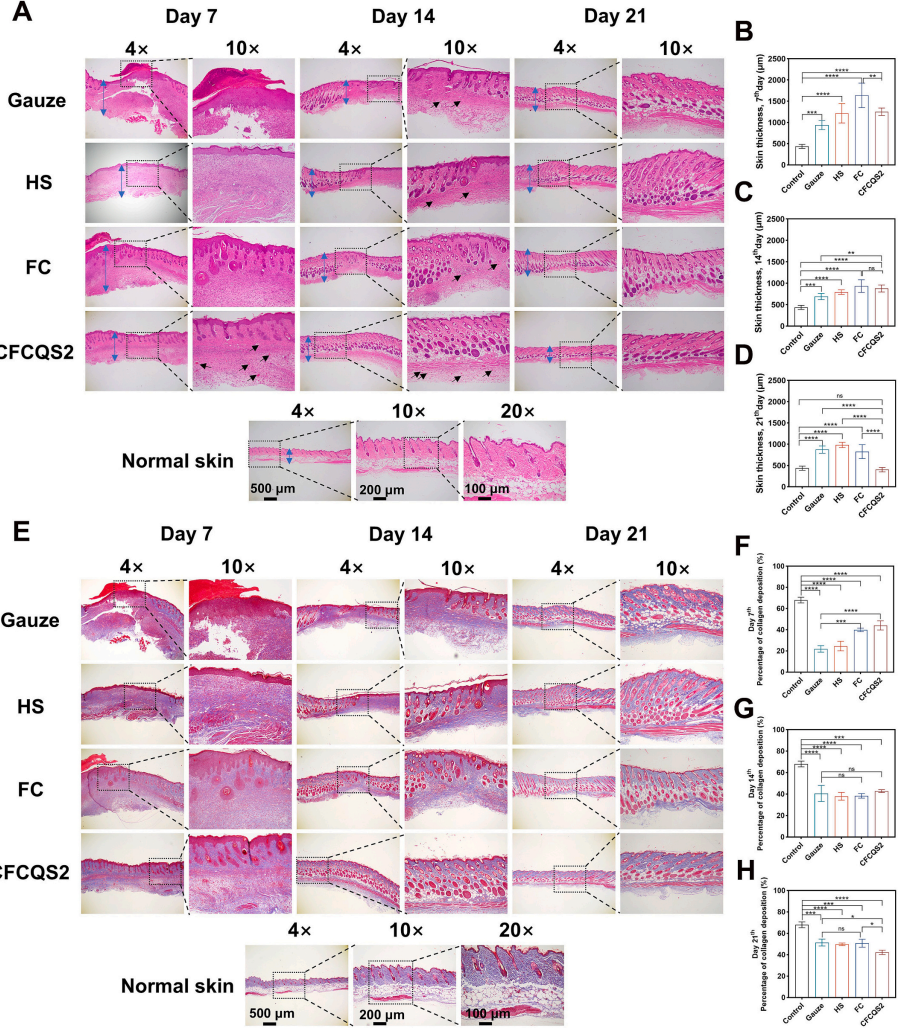
图5 敷料干预治疗后的基本病理染色分析。(A) 用不同敷料处理的伤口的H&E染色。(B–D) 第7、14和21天小鼠伤口部位的皮肤厚度。(E) 用不同敷料处理的伤口的Masson染色显微照片。(F–H) 第7、14和21天小鼠伤口部位胶原蛋白沉积的百分比。(ns表示无显著差异,*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001)。
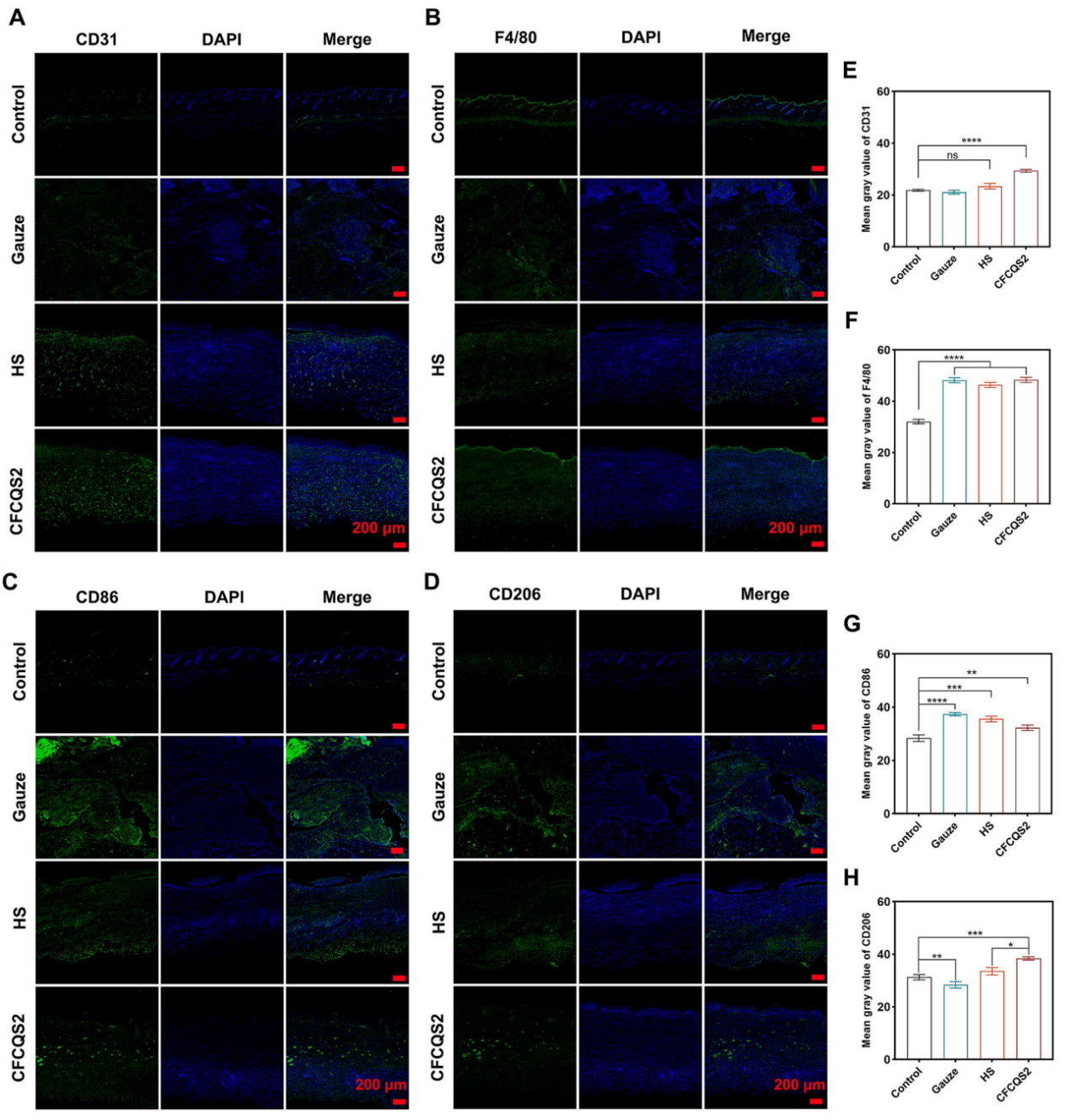
图6. 治疗后第7天伤口组织中血管生成和巨噬细胞极化的免疫荧光分析。(A) CD31染色(绿色)表明血管内皮细胞和新血管形成。(B) F4/80染色(绿色)显示巨噬细胞整体浸润。(C) CD86染色(绿色),M1型促炎巨噬细胞的标记。(D) CD206染色(绿色),M2型抗炎巨噬细胞的标记。细胞核用DAPI(蓝色)复染。(E) CD31的平均灰度值。(F) F4/80的平均灰度值。(G) CD86的平均灰度值。(H) CD206的平均灰度值。(ns表示无显著差异,*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001)。
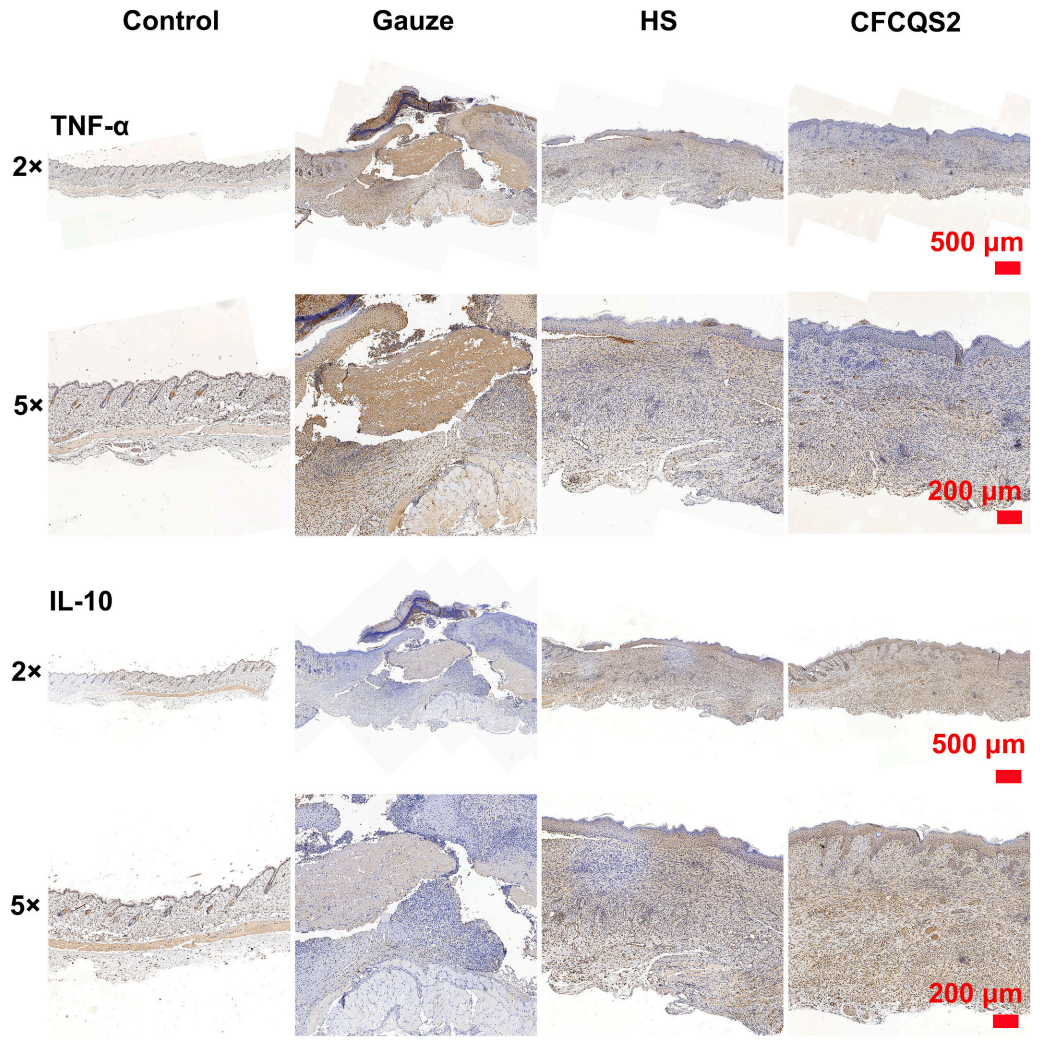
图7. 治疗后第7天伤口组织中TNF-α和IL-10的免疫组织化学染色。(A) 2倍和 5倍放大倍数下的TNF-α表达(棕色),表明局部炎症水平。(B) 2倍和5倍放大倍数下的IL-10表达(棕色),表明具有抗炎活性。在所有组中,CFCQS2治疗组表现出最低的TNF-α和最高的IL-10表达,表明促炎反应受到抑制并促进M2巨噬细胞相关组织修复。
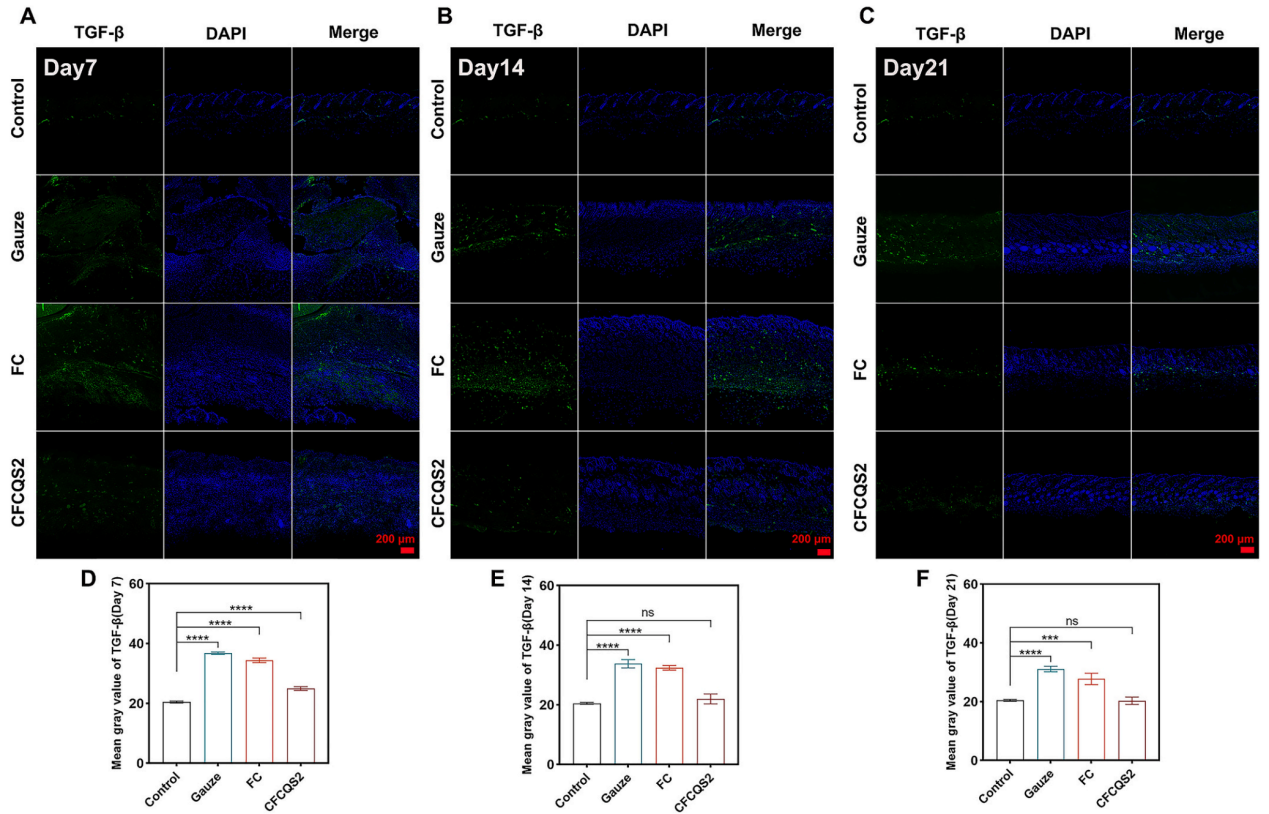
图8. 损伤后(A) 第7天 (B) 第14天 (C) 第21天伤口组织中TGF-β表达的免疫荧光染色。(D) 第7天TGF-β的平均灰度值。(E) 第14天TGF-β的平均灰度值。(F) 第21天TGF-β的平均灰度值。TGF-β(绿色)和DAPI核染色(蓝色)用于评估纤维化相关细胞因子的表达。纱布组和FC组在所有时间点都表现出升高的TGF-β水平,而CFCQS2组表现出TGF-β表达降低,与对照组相当,表明纤维化反应减弱。(ns表示无显著差异,***p < 0.001,****p < 0.0001)。
研究总结与展望
本研究成功开发了一种具有皮肤温度激活形状记忆功能的双层伤口敷料(CFCQS2),其外层PLATMC纤维膜在体温下自发收缩提供机械闭合力,内层胶原蛋白/季铵化硅酮海绵则赋予主动抗菌、快速止血及免疫调节功能;体内实验证实,该敷料通过促进血管生成、驱动巨噬细胞向M2型极化以及调控TNF-α、IL-10和TGF-β等关键因子,实现了感染伤口的快速闭合与有序胶原沉积的无瘢痕修复。未来研究将重点阐明其免疫调节与抑制瘢痕的具体分子机制,并进一步验证材料的长期生物相容性、体内降解动力学及规模化生产潜力,以推动其临床转化应用。
山东医药大学硕士研究生齐钦兵为论文第一作者;侯桂革教授和李诚博博士为共同通讯作者。该研究得到了国家自然科学基金、山东省重点实验室计划、山东省自然科学基金、山东省高校青年创新科技支撑计划、山东省高等学校“青年创新团队计划”的资助基金项目、山东省科技型中小企业创新能力提升项目、山东省卫生技术创新团队建设项目、烟台市科技创新发展计划基础研究项目的支持,在此一并致谢。
原文链接:https://doi.org/10.1016/j.cej.2026.176523.


