我院精准医学团队以滨州医学院为第一署名单位和通讯作者单位,近期在国际权威期刊《Theranostics》(中科院JCR一区,2024年影响因子:12.4)杂志上在线发表题为“MRI guided copper deprivator activated immune responses and suppressed angiogenesis for enhanced antitumor immunotherapy”的最新研究成果。我院硕士研究生王银凤、王鹏和李慧敏为论文共同第一作者,高文娟副教授和张桂龙教授为该文章共同通讯作者,上海交大九院和安徽医科大一附院为共同通讯单位。
近年来研究发现铜通过调节程序性死亡配体1(PD-L1)的表达,参与调控肿瘤免疫逃逸。这表明,干预肿瘤内部的铜含量,有望成为一种增强抗肿瘤免疫治疗效果的潜在途径。
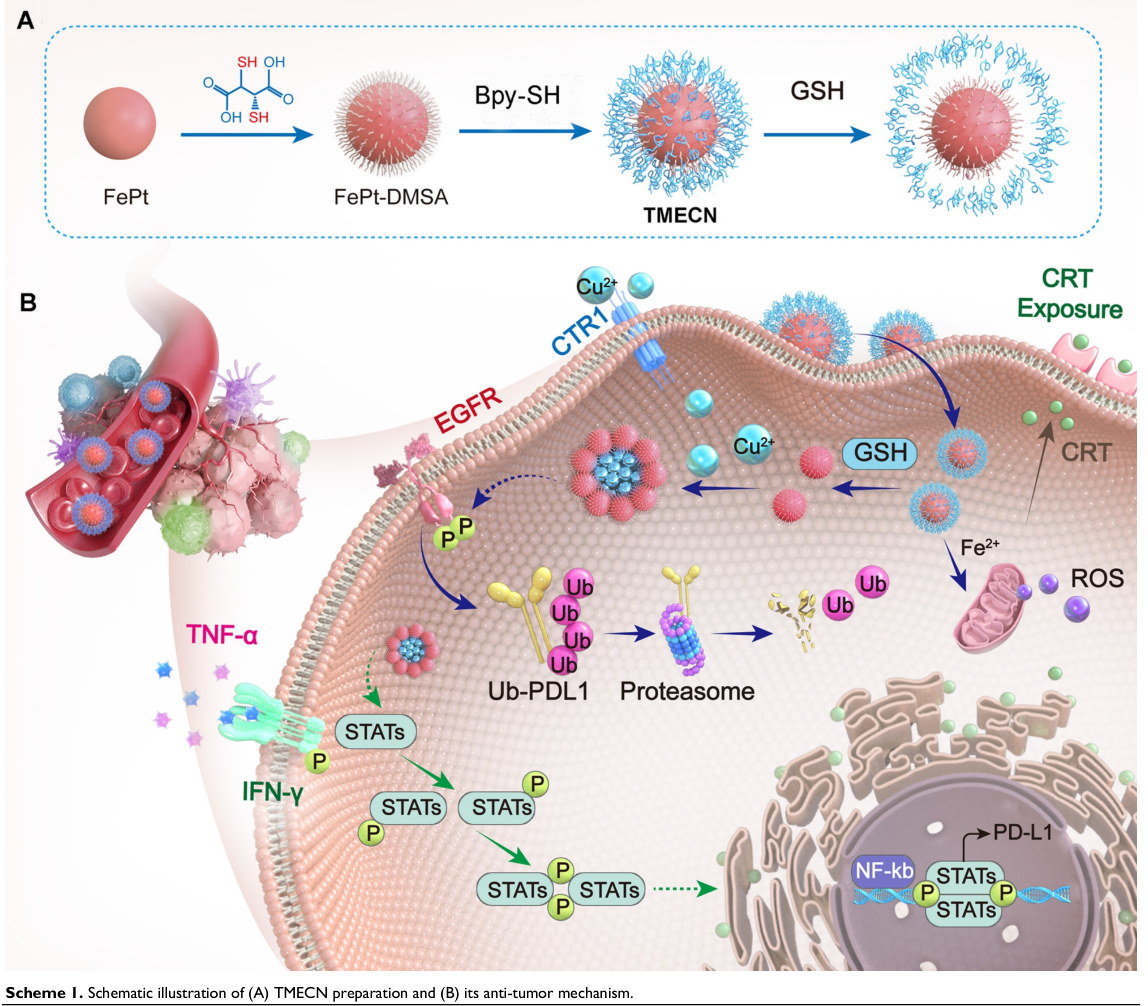
基于此,研究人员开发了一种肿瘤微环境响应型铜纳米剥夺剂(TMECN),通过巯基聚乙二醇联吡啶与二巯基丁二酸利用二硫键修饰铂铁(FePt)纳米合金的交联作用,来增强肿瘤的免疫治疗效果。当TMECN进入肿瘤细胞后,其内部的二硫键会被过度表达的谷胱甘肽切断,从而暴露出大量的巯基。接下来,TMECN会主动捕获癌细胞中的铜离子,引发TMECN的自组装。铜含量的降低不仅抑制了肿瘤新生血管生成和PD-L1的转录,还促进了PD-L1的泛素化降解,从而阻断了肿瘤的免疫逃逸。此外,TMECN能催化芬顿反应,并在癌细胞中产生活性氧,诱导肿瘤发生免疫原性细胞死亡。对PD-L1的抑制和对免疫原性细胞死亡的激活协同促进了细胞毒性T淋巴细胞向肿瘤的浸润,引发了强烈的抗肿瘤免疫反应,最终抑制了肿瘤的生长和转移。另外,TMECN在肿瘤中的自组装诱导了从T1到T2的可切换对比成像,显著提高了肿瘤的精准诊断水平。总的来说,该项目将为增强磁共振成像(MRI)引导的抗肿瘤免疫治疗提供一种新的策略。
该研究得到了国家自然科学基金、泰山学者人才工程项目、山东省重点研发计划项目、山东省自然科学基金青年项目、滨州医学院科研启动基金等项目的支持,在此一并致谢。
原文链接:https://doi: 10.7150/thno.102556. eCollection 2025.


