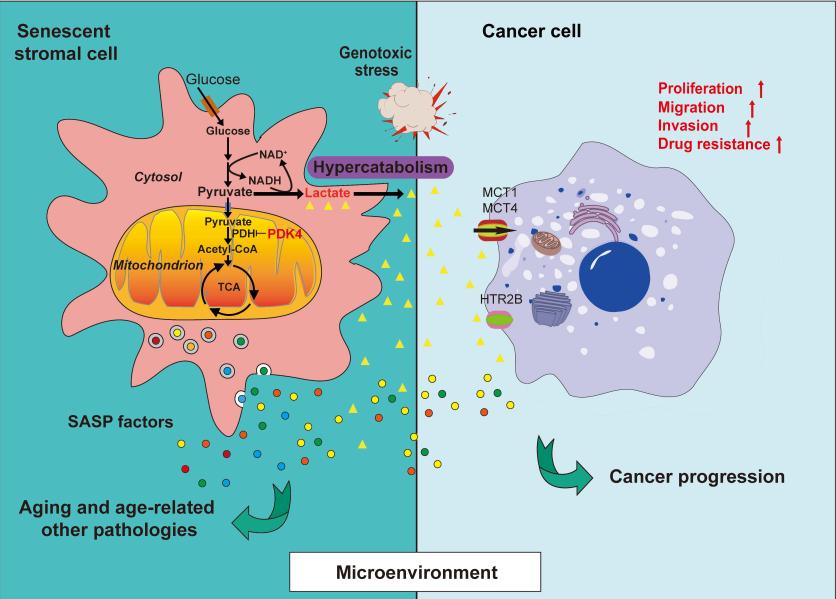
近日,滨州医学院药学院孙宇教授带领的衰老医学研究所团队与中国科学院大学上海营养与健康研究所合作成果“PDK4-dependent hypercatabolism and lactate production of senescence cells promotes cancer malignancy”发表在Nature子刊《Nature Metabolism》。该研究揭示了衰老相关分泌表型(SASP)广谱表达的同时,丙酮酸脱氢酶激酶4(PDK4)在衰老细胞中显著上调,后者可以介导衰老细胞代谢重编程并使其呈现一种葡萄糖高分解代谢的特性。
在深度分析衰老细胞的表达特征和代谢活性时,团队注意到与葡萄糖分解代谢有关的蛋白酶PDK4在细胞衰老过程中显著上调,并且在不同类型衰老细胞中均普遍出现。在表达规律上,PDK4跟大多数SASP因子几乎同步上调,此后基本维持在一个平台期,并且在基质细胞中的幅度显著高于癌细胞。在对临床肿瘤样本进行分析时,发现化疗后阶段癌症患者病灶中PDK4的表达水平同组织中的细胞衰老程度直接相关,并跟疗后阶段癌症患者的生存期之间负相关。这些数据表明,PDK4在衰老细胞群中的表达可能具有重要的病理意义。
研究人员进而发现:与增殖细胞相比,衰老细胞的糖酵解强度和TCA循环活性均发生了深刻变化。与葡萄糖酵解密切相关的代谢物产量均有上升,表明衰老细胞能进一步利用一些中间代谢物。一些酵解支路和TCA循环相关的基因普遍在衰老细胞中上调表达。在基于荷瘤小鼠的预临床试验中,发现衰老细胞的存在加速了肿瘤进展,但敲除PDK4之后这一趋势则被明显抑制。当PDK4-IN与MIT联合使用时,研究人员观察到肿瘤进一步缩小。组织学分析表明,接受MIT治疗的小鼠肿瘤组织中SA-β-GAL阳性水平升高,但PDK4-IN给药则导致SA-β-GAL阳性率降低,暗示PDK4可能会促进化疗条件下动物体内衰老进程。
预临床条件下MIT给药后,典型的凋亡指标尤其caspase 3自裂解增加,而PDK4-IN与MIT联用则进一步增强了这一趋势。将PDK4靶向药物与经典化疗相结合可增强肿瘤对治疗的反应,而不会引起严重的全身性细胞毒效应,肝肾等主要器官功能未受影响,说明这一组合方案的可行性和安全性,具有将来向临床转化和推广应用的良好前景。
本项研究工作系统解析了细胞衰老、乳酸生成、器官退行和增龄相关疾病之间的关联,并开创了相应的干预策略。滨州医学院孙宇教授、华东理工大学药学院赵玉政教授为该论文共同通讯作者。中国科学院上海营养与健康研究所窦雪峰博士、滨州医学院付强教授以及复旦大学附属中山医院泌尿外科龙启来博士为该论文共同第一作者。美国Buck衰老研究所Judith Campisi和滨州医学院张桂龙等人提供了大力协助。该工作得到国家重点研发计划、国家自然科学基金、中国科学院战略先导科技专项、山东省泰山学者人才工程、烟台市双百人才计划以及中国科学院上海营养与健康研究所所级公共技术平台的支持。原文链接:https://www.nature.com/articles/s42255-023-00912-w


